Đề bài
Cho các phản ứng :
(a) Ca(OH)2 + CO2 → CaCO3 + H2O
(b) 2H2S + SO2 → 3S + 2H2O
(c) 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O
(d) 4KClO3 → KCl + 3KClO4
Số phản ứng oxi hóa - khử là :
-
A.
2
-
B.
4
-
C.
3
-
D.
1
Chất nào dưới đây thể hiện tính khử khi cho tác dụng với dung dịch H2SO4 loãng?
-
A.
Fe.
-
B.
Fe(OH)2.
-
C.
FeO.
-
D.
FeCl3.
Phát biểu nào dưới đây không đúng?
-
A.
Sự oxi hóa là sự mất (nhường) electron
-
B.
Sự khử là sự mất electron hay cho electron
-
C.
Chất khử là chất nhường (cho) electron
-
D.
Chất oxi hóa là chất thu electron
Cho phản ứng: Mg + H2SO4 → MgSO4 + S + H2O. Tổng hệ số cân bằng là:
-
A.
18
-
B.
16
-
C.
20
-
D.
15
Phản ứng nào dưới đây thuộc loại phản ứng oxi hóa khử?
-
A.
NaOH + HBr → NaBr + H2O.
-
B.
3NO2 + H2O → 2HNO3 + NO.
-
C.
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4.
-
D.
O3 → O2 + O.
Dấu hiệu để nhận biết một phản ứng oxi hóa – khử là:
-
A.
Có tạo ra chất khí.
-
B.
Có sự thay đổi số oxi hóa của một số nguyên tố.
-
C.
Có sự thay đổi màu sắc của các chất.
-
D.
Có tạo ra chất kết tủa.
Cho phương trình hóa học : 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3. Kết luận nào sau đây là đúng?
-
A.
Fe(OH)2 là chất khử, H2O là chất oxi hoá.
-
B.
Fe(OH)2 là chất khử, O2 là chất oxi hoá.
-
C.
O2 là chất khử, H2O là chất oxi hoá.
-
D.
Fe(OH)2 là chất khử, O2 và H2O là chất oxi hoá
Cho quá trình sau: $\overset{+\text{3}}{\mathop{\text{Fe}}}\,$ + 1e → $\overset{+\text{2}}{\mathop{\text{Fe}}}\,$. Trong các kết luận sau, kết luận nào là đúng?
-
A.
Quá trình trên là quá trình oxi hóa.
-
B.
Quá trình trên là quá trình khử.
-
C.
Trong quá trình trên $\overset{+\text{3}}{\mathop{\text{Fe}}}\,$ đóng vai trò là chất khử.
-
D.
Trong quá trình trên $\overset{+\text{2}}{\mathop{\text{Fe}}}\,$ đóng vai trò là chất oxi hóa.
Cho amoniac NH3 tác dụng với oxi ở nhiệt độ cao có xúc tác thích hợp sinh ra nitơ oxit NO và nước. Phương trình hoá học: 4NH3 + 5O2 → 4NO + 6H2O. Trong phản ứng trên, NH3 đóng vai trò
-
A.
là chất oxi hoá.
-
B.
là chất khử.
-
C.
là một bazơ.
-
D.
là một axit.
Cho sơ đồ phản ứng: FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + 5NO + H2O
Sau khi cân bằng, tổng hệ số cân bằng của phản ứng là
-
A.
25
-
B.
21
-
C.
23
-
D.
19
Cho khí CO dư đi qua ống sứ chứa Fe2O3 và MgO nung nóng, sau khi phản ứng xảy ra hoàn toàn thu dược chất rắn X. Cho X vào dung dịch FeCl3 và CuCl2, thu được chất rắn Y. Cho Y tác dụng với dung dịch HCl dư, thu được dung dịch Z chứa ba chất tan. Dãy gồm các chất nào sau đây khi tác dụng với Z đều có phản ứng xảy ra pahrn ứng oxi hóa - khử?
-
A.
Cl2, NaOH, K2Cr2O7.
-
B.
AgNO3, Cl2, KNO3.
-
C.
H2S, NaOH, AgNO3.
-
D.
AgNO3, NH3, KMnO4.
Cho phản ứng: KMnO4 + FeSO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
Hệ số của chất oxi hóa và chất khử trong phản ứng trên lần lượt là
-
A.
5 và 1.
-
B.
2 và 10.
-
C.
1 và 5.
-
D.
5 và 2.
Ở phản ứng nào sau đây, H2O không đóng vai trò chất oxi hoá hay chất khử?
-
A.
NaH + H2O → NaOH + H2
-
B.
2Na + 2H2O → 2NaOH + H2
-
C.
2F2 + 2H2O → 4HF + O2
-
D.
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
Cho phản ứng: aCu + bHNO3 → cCu(NO3)2 + dNO + eH2O
Với a, b, c, d, e là những số nguyên tối giản. Tổng (a+b) bằng?
-
A.
5
-
B.
8
-
C.
11
-
D.
12
Dấu hiệu để nhận biết một phản ứng oxi hóa – khử là
-
A.
tạo ra chất khí.
-
B.
tạo ra chất kết tủa.
-
C.
có sự thay đổi màu sắc của các chất.
-
D.
có sự thay đổi số oxi hóa của một số nguyên tố.
Chọn phát biểu đúng trong các phát biểu sau ?
-
A.
Chất oxi hóa là chất nhường electron.
-
B.
Quá trình nhận electron là quá trình oxi hóa.
-
C.
Chất khử là chất nhận electron.
-
D.
Quá trình nhường electron là quá trình oxi hóa.
Trong phản ứng : Cl2 + 2KBr → Br2 + 2KCl, nguyên tố clo…
-
A.
chỉ bị khử.
-
B.
không bị oxi hóa, không bị khử.
-
C.
chỉ bị oxi hóa.
-
D.
vừa bị oxi hóa, vừa bị khử.
Quá trình nào sau đây là đúng
-
A.
\(\;\mathop {Al}\limits^0 + 3e\; \to \mathop {Al}\limits^{ + 3} \)
-
B.
\(\;\mathop {Mn}\limits^{ + 7} + 4e\; \to \mathop {Mn}\limits^{ + 4} \)
-
C.
\(\;\mathop S\limits^{ - 2} \; \to \mathop S\limits^0 + 2e\)
-
D.
\(\;\mathop {Mn}\limits^{ + 4} + 3e\; \to \mathop {Mn}\limits^{ + 7} \)
Cho quá trình NO3- + 3e + 4H+ → NO + 2H2O, đây là quá trình
-
A.
nhận proton.
-
B.
oxi hóa.
-
C.
khử.
-
D.
tự oxi hóa – khử.
Dấu hiệu để nhận biết một phản ứng oxi hóa khử:
-
A.
Tạo ra chất kết tủa
-
B.
Tạo ra chất khí
-
C.
Có sự thay đổi màu sắc của các chất
-
D.
Có sự thay đổi số oxi hóa của một số nguyên tử
Trong các phản ứng hóa học, SO2 có thể là chất oxi hoá hoặc chất khử vì
-
A.
lưu huỳnh trong SO2 đã đạt số oxi hóa cao nhất.
-
B.
SO2 là oxit axit.
-
C.
lưu huỳnh trong SO2 có số oxi hóa trung gian.
-
D.
SO2 tan được trong nước.
Cho các chất và ion sau: Zn, S, FeO, ZnO, SO2, Fe2+, Cu2+, HCl. Tổng số phân tử và ion trong dãy vừa có tính oxi hóa, vừa có tính khử là
-
A.
5.
-
B.
6.
-
C.
7.
-
D.
8.
Loại phản ứng nào sau đây luôn không phải là phản úng oxi hóa – khử ?
-
A.
Phản ứng phân hủy
-
B.
Phản ứng trao đổi
-
C.
Phản ứng thế trong hóa học vô cơ
-
D.
Phản ứng hóa học
Hòa tan 12,6 gam Fe bằng dung dịch H2SO4 loãng dư, thu được dung dịch X. Dung dịch X phản ứng vừa đủ với V ml dung dịch KMnO4 0,5M. Giá trị của V là
-
A.
180.
-
B.
90
-
C.
45
-
D.
135
Trong phản ứng đốt cháy CuFeS2 tạo ra các sản phẩm CuO, Fe2O3 và SO2 thì 1 phân tử CuFeS2 sẽ
-
A.
nhường 13e.
-
B.
nhận 12e.
-
C.
nhận 13e.
-
D.
nhường 12e.
Cho 29,6 gam hỗn hợp X gồm Fe, Mg, Cu theo tỉ lệ mol 1 : 2 : 3 bằng H2SO4 đặc nguội được dung dịch Y và 11,2 lít SO2 (đktc). Cô cạn dung dịch Y được khối lượng muối khan là
-
A.
72 gam
-
B.
21,2 gam
-
C.
43,4 gam
-
D.
36,5 gam
Một hỗn hợp gồm hai bột kim loại Mg và Al được chia thành hai phần bằng nhau:
- Phần 1: cho tác dụng với HCl dư thu được 3,36 lít H2.
- Phần 2: hoà tan hết trong HNO3 loãng dư thu được V lít một khí không màu, hoá nâu trong không khí .
Biết các thể tích khí đều đo ở đktc, giá trị của V là
-
A.
2,24 lít.
-
B.
3,36 lít.
-
C.
4,48 lít.
-
D.
5,6 lít.
Điện phân nóng chảy muối clorua kim loại kiềm, thu được 0,896 lít khí (đktc) và 3,12 gam kim loại. Công thức của muối là:
-
A.
LiCl
-
B.
KCl
-
C.
NaCl
-
D.
RbCl
Cho 15,2 gam hỗn hợp X gồm Mg và Ca phản ứng vừa đủ với 8,96 lít (đktc) hỗn hợp khí Y gồm Cl2 và O2 thu được 39,7 gam chất rắn Z chỉ gồm các muối clorua và các oxit kim loại. Khối lượng của Mg trong 15,2 gam X là
-
A.
4,8 gam.
-
B.
7,2 gam.
-
C.
9,2 gam.
-
D.
3,6 gam.
Hòa tan hoàn toàn m gam Al vào dung dịch HNO3 loãng, dư thu được 1,344 lít khí N2 (đktc) và dung dịch X. Thêm NaOH dư vào dung dịch X và đun sôi thì thu được 1,344 lít khí NH3 (đktc). Giá trị của m là:
-
A.
0,54
-
B.
1,62
-
C.
10,08
-
D.
9,72
Lời giải và đáp án
Cho các phản ứng :
(a) Ca(OH)2 + CO2 → CaCO3 + H2O
(b) 2H2S + SO2 → 3S + 2H2O
(c) 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O
(d) 4KClO3 → KCl + 3KClO4
Số phản ứng oxi hóa - khử là :
-
A.
2
-
B.
4
-
C.
3
-
D.
1
Đáp án : C
Dựa vào khái niệm về phản ứng oxi hóa – khử: Phản ứng oxi hóa – khử là phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
Các phản ứng oxi hóa – khử là (b), (c), (d)
Chất nào dưới đây thể hiện tính khử khi cho tác dụng với dung dịch H2SO4 loãng?
-
A.
Fe.
-
B.
Fe(OH)2.
-
C.
FeO.
-
D.
FeCl3.
Đáp án : A
Chất khử là chất nhường e để lên mức oxi hóa cao hơn.
Chất khử là chất nhường e để lên mức oxi hóa cao hơn.
Fe + H2SO4 → FeSO4 + H2 => Fe thể hiện tính khử
Phát biểu nào dưới đây không đúng?
-
A.
Sự oxi hóa là sự mất (nhường) electron
-
B.
Sự khử là sự mất electron hay cho electron
-
C.
Chất khử là chất nhường (cho) electron
-
D.
Chất oxi hóa là chất thu electron
Đáp án : B
Nắm được khái niệm:
+ Chất khử là chất nhường e
+ Chất oxi hóa là chất nhận e
+ Sự khử là sự nhận e
+ Sự oxi hóa là sự nhường e
B sai vì sự khử là sự nhận e
Cho phản ứng: Mg + H2SO4 → MgSO4 + S + H2O. Tổng hệ số cân bằng là:
-
A.
18
-
B.
16
-
C.
20
-
D.
15
Đáp án : D
Cân bằng phản ứng oxi hóa – khử bằng phương pháp thăng bằng electron.
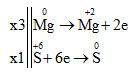
3Mg + 4H2SO4 → 3MgSO4 + S + 4H2O
Tổng hệ số cân bằng là: 3 + 4 + 3 + 1 + 4 = 15
Phản ứng nào dưới đây thuộc loại phản ứng oxi hóa khử?
-
A.
NaOH + HBr → NaBr + H2O.
-
B.
3NO2 + H2O → 2HNO3 + NO.
-
C.
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4.
-
D.
O3 → O2 + O.
Đáp án : B
Phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của nguyên tố.
\(3\mathop N\limits^{ + 4} {O_2} + {H_2}O \to 2H\mathop N\limits^{ + 5} {O_3} + \mathop N\limits^{ + 2} O\)
Dấu hiệu để nhận biết một phản ứng oxi hóa – khử là:
-
A.
Có tạo ra chất khí.
-
B.
Có sự thay đổi số oxi hóa của một số nguyên tố.
-
C.
Có sự thay đổi màu sắc của các chất.
-
D.
Có tạo ra chất kết tủa.
Đáp án : B
Phản ứng oxi hóa khử là phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
Cho phương trình hóa học : 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3. Kết luận nào sau đây là đúng?
-
A.
Fe(OH)2 là chất khử, H2O là chất oxi hoá.
-
B.
Fe(OH)2 là chất khử, O2 là chất oxi hoá.
-
C.
O2 là chất khử, H2O là chất oxi hoá.
-
D.
Fe(OH)2 là chất khử, O2 và H2O là chất oxi hoá
Đáp án : B
$4\overset{+2}{\mathop{Fe}}\,{{\left( OH \right)}_{2}}~+~{{\overset{0}{\mathop{O}}\,}_{2}}~+\text{ }2{{H}_{2}}O\text{ }\to \text{ }4\overset{+3}{\mathop{Fe}}\,{{(\overset{-2}{\mathop{O}}\,H)}_{3}}.$
Quá trình cho – nhận e:
$\overset{+2}{\mathop{Fe}}\,~\,\,\to \text{ }\overset{+3}{\mathop{Fe}}\,\,\,+\,\,1\text{e}$ => Fe(OH)2 là chất khử
${{\overset{0}{\mathop{O}}\,}_{2}}~+\text{ 4e }\to \text{ 2}\overset{-2}{\mathop{O}}\,$ => O2 là chất oxi hóa
Cho quá trình sau: $\overset{+\text{3}}{\mathop{\text{Fe}}}\,$ + 1e → $\overset{+\text{2}}{\mathop{\text{Fe}}}\,$. Trong các kết luận sau, kết luận nào là đúng?
-
A.
Quá trình trên là quá trình oxi hóa.
-
B.
Quá trình trên là quá trình khử.
-
C.
Trong quá trình trên $\overset{+\text{3}}{\mathop{\text{Fe}}}\,$ đóng vai trò là chất khử.
-
D.
Trong quá trình trên $\overset{+\text{2}}{\mathop{\text{Fe}}}\,$ đóng vai trò là chất oxi hóa.
Đáp án : B
Quá trình nhận electron gọi là quá trình khử (sự khử)
Cho amoniac NH3 tác dụng với oxi ở nhiệt độ cao có xúc tác thích hợp sinh ra nitơ oxit NO và nước. Phương trình hoá học: 4NH3 + 5O2 → 4NO + 6H2O. Trong phản ứng trên, NH3 đóng vai trò
-
A.
là chất oxi hoá.
-
B.
là chất khử.
-
C.
là một bazơ.
-
D.
là một axit.
Đáp án : B
$4\overset{-3}{\mathop{N}}\,{{H}_{3}}+\text{ }5{{\overset{0}{\mathop{O}}\,}_{2}}\to 4\overset{+2}{\mathop{N}}\,\overset{-2}{\mathop{O}}\,\text{ }+\text{ }6{{H}_{2}}O$
Quá trình cho – nhận e của N:
$\mathop N\limits^{ - 3} {\mkern 1mu} {H_3}{\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} {\text{}} \to {\mkern 1mu} {\mkern 1mu} {\mkern 1mu} \mathop N\limits^{ + 2} {\mkern 1mu} O{\mkern 1mu} {\mkern 1mu} $ + 5e
=> NH3 đóng vai trò là chất khử.
Cho sơ đồ phản ứng: FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + 5NO + H2O
Sau khi cân bằng, tổng hệ số cân bằng của phản ứng là
-
A.
25
-
B.
21
-
C.
23
-
D.
19
Đáp án : D
Cân bằng phản ứng oxi hóa khử theo phương pháp thăng bằng electron.
FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
Tổng hệ số cân bằng của phản ứng là: 1 + 8 + 1 + 2 + 5 + 2 = 19
Đáp án D
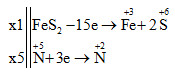
FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
Tổng hệ số cân bằng của phản ứng là: 1 + 8 + 1 + 2 + 5 + 2 = 19
Cho khí CO dư đi qua ống sứ chứa Fe2O3 và MgO nung nóng, sau khi phản ứng xảy ra hoàn toàn thu dược chất rắn X. Cho X vào dung dịch FeCl3 và CuCl2, thu được chất rắn Y. Cho Y tác dụng với dung dịch HCl dư, thu được dung dịch Z chứa ba chất tan. Dãy gồm các chất nào sau đây khi tác dụng với Z đều có phản ứng xảy ra pahrn ứng oxi hóa - khử?
-
A.
Cl2, NaOH, K2Cr2O7.
-
B.
AgNO3, Cl2, KNO3.
-
C.
H2S, NaOH, AgNO3.
-
D.
AgNO3, NH3, KMnO4.
Đáp án : B
Sơ đồ:\(CO + \left\{ \matrix{
F{e_2}{O_3} \hfill \cr
MgO \hfill \cr} \right.\buildrel {{t^0}} \over
\longrightarrow X\left\{ \matrix{
Fe \hfill \cr
MgO \hfill \cr} \right.\buildrel { + FeC{l_3},CuC{l_2}} \over
\longrightarrow ran\,Y\left\{ \matrix{
Fe \hfill \cr
Cu \hfill \cr
MgO \hfill \cr} \right.\buildrel { + HCl\,du} \over
\longrightarrow ddZ\left\{ \matrix{
FeC{l_2} \hfill \cr
MgC{l_2} \hfill \cr
HCldu \hfill \cr} \right.\)
Dựa vào đáp án chọn đáp án phù hợp
\(CO + \left\{ \matrix{
F{e_2}{O_3} \hfill \cr
MgO \hfill \cr} \right.\buildrel {{t^0}} \over
\longrightarrow X\left\{ \matrix{
Fe \hfill \cr
MgO \hfill \cr} \right.\buildrel { + FeC{l_3},CuC{l_2}} \over
\longrightarrow rắn\,Y\left\{ \matrix{
Fe \hfill \cr
Cu \hfill \cr
MgO \hfill \cr} \right.\buildrel { + HCl\,dư} \over
\longrightarrow ddZ\left\{ \matrix{
FeC{l_2} \hfill \cr
MgC{l_2} \hfill \cr
HCldu \hfill \cr} \right.\)
A. Loại NaOH không có phản ứng oxh- khử
B. Thỏa mãn
Ag+ + Fe2+ → Fe3+ + Ag↓
3Fe2+ + NO3- + 4H+ → 3Fe3+ + NO + 2H2O
Cl2 + Fe2+ → Fe3+ + Cl-
C. Loại NaOH không có phản ứng oxh- khử
D. Loại NH3 không có phản ứng oxh- khử
Cho phản ứng: KMnO4 + FeSO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
Hệ số của chất oxi hóa và chất khử trong phản ứng trên lần lượt là
-
A.
5 và 1.
-
B.
2 và 10.
-
C.
1 và 5.
-
D.
5 và 2.
Đáp án : B
Cân bằng phản ứng oxi hóa khử bằng phương pháp thăng bằng electron.
Chất khử là chất cho e, chất oxi hóa là chất nhận e.
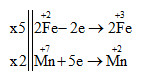
2KMnO4 + 10FeSO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Chất oxi hóa là KMnO4 có hệ số là 2
Chất khử là FeSO4 có hệ số là 10
Ở phản ứng nào sau đây, H2O không đóng vai trò chất oxi hoá hay chất khử?
-
A.
NaH + H2O → NaOH + H2
-
B.
2Na + 2H2O → 2NaOH + H2
-
C.
2F2 + 2H2O → 4HF + O2
-
D.
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
Đáp án : D
Xem lại định nghĩa phản ứng oxi hóa – khử (c3)
H2O không đóng vai trò chất oxi hoá hay chất khử => H2O không thay đổi số oxi hóa
$A{{l}_{4}}{{C}_{3}}+\text{ }12{{\overset{+1}{\mathop{H}}\,}_{2}}\overset{-2}{\mathop{O}}\,\to 4Al{{(\overset{-2}{\mathop{O}}\,\overset{+1}{\mathop{H}}\,)}_{3}}+\text{ }3C{{\overset{+1}{\mathop{H}}\,}_{4}}$
Cho phản ứng: aCu + bHNO3 → cCu(NO3)2 + dNO + eH2O
Với a, b, c, d, e là những số nguyên tối giản. Tổng (a+b) bằng?
-
A.
5
-
B.
8
-
C.
11
-
D.
12
Đáp án : C
Cân bằng phản ứng oxi hóa khử theo phương pháp thăng bằng e.
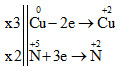
Vậy 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Tổng a + b = 3 + 8 = 11
Dấu hiệu để nhận biết một phản ứng oxi hóa – khử là
-
A.
tạo ra chất khí.
-
B.
tạo ra chất kết tủa.
-
C.
có sự thay đổi màu sắc của các chất.
-
D.
có sự thay đổi số oxi hóa của một số nguyên tố.
Đáp án : D
Phản ứng oxi hóa khử là phản ứng có sự thay đổi số oxi hóa của một hay nhiều nguyên tố.
Chọn phát biểu đúng trong các phát biểu sau ?
-
A.
Chất oxi hóa là chất nhường electron.
-
B.
Quá trình nhận electron là quá trình oxi hóa.
-
C.
Chất khử là chất nhận electron.
-
D.
Quá trình nhường electron là quá trình oxi hóa.
Đáp án : D
- Ghi nhớ câu “khử cho – o nhận”
+ Chất khử là chất cho e (bị oxi hóa)
+ Chất oxi hóa là chất nhận e (bị khử)
- Quá trình cho e là quá trình oxi hóa, quá trình nhận e là quá trình khử.
Phát biểu đúng là “quá trình nhường electron là quá trình oxi hóa.”
Trong phản ứng : Cl2 + 2KBr → Br2 + 2KCl, nguyên tố clo…
-
A.
chỉ bị khử.
-
B.
không bị oxi hóa, không bị khử.
-
C.
chỉ bị oxi hóa.
-
D.
vừa bị oxi hóa, vừa bị khử.
Đáp án : A
- Xác định số oxi hóa của Cl trước và sau phản ứng
- Xác định vai trò của Cl:
+ Chất nhường e là chất khử
+ Chất nhận e là chất oxi hóa
\(C{l_2} + 2e \to 2\mathop {Cl}\limits^{ - 1} \)
Cl2 nhận e nên là chất oxi hóa
Quá trình nào sau đây là đúng
-
A.
\(\;\mathop {Al}\limits^0 + 3e\; \to \mathop {Al}\limits^{ + 3} \)
-
B.
\(\;\mathop {Mn}\limits^{ + 7} + 4e\; \to \mathop {Mn}\limits^{ + 4} \)
-
C.
\(\;\mathop S\limits^{ - 2} \; \to \mathop S\limits^0 + 2e\)
-
D.
\(\;\mathop {Mn}\limits^{ + 4} + 3e\; \to \mathop {Mn}\limits^{ + 7} \)
Đáp án : C
Quá trình đúng là: \(\;\mathop S\limits^{ - 2} \; \to \mathop S\limits^0 + 2e\)
Cho quá trình NO3- + 3e + 4H+ → NO + 2H2O, đây là quá trình
-
A.
nhận proton.
-
B.
oxi hóa.
-
C.
khử.
-
D.
tự oxi hóa – khử.
Đáp án : C
Ta thấy quá trình trên là quá trình nhận e nên là quá trình khử.
Dấu hiệu để nhận biết một phản ứng oxi hóa khử:
-
A.
Tạo ra chất kết tủa
-
B.
Tạo ra chất khí
-
C.
Có sự thay đổi màu sắc của các chất
-
D.
Có sự thay đổi số oxi hóa của một số nguyên tử
Đáp án : D
Phản ứng oxi hóa - khử là phản ứng có sự thay đổi số oxi hóa của một số nguyên tố
Trong các phản ứng hóa học, SO2 có thể là chất oxi hoá hoặc chất khử vì
-
A.
lưu huỳnh trong SO2 đã đạt số oxi hóa cao nhất.
-
B.
SO2 là oxit axit.
-
C.
lưu huỳnh trong SO2 có số oxi hóa trung gian.
-
D.
SO2 tan được trong nước.
Đáp án : C
Chất khử cho e, chất oxi hóa nhận e => chất vừa có khả năng cho e, vừa có khả năng nhận e
SO2 có thể là chất oxi hoá hoặc chất khử vì lưu huỳnh trong SO2 có số oxi hóa trung gian.
Cho các chất và ion sau: Zn, S, FeO, ZnO, SO2, Fe2+, Cu2+, HCl. Tổng số phân tử và ion trong dãy vừa có tính oxi hóa, vừa có tính khử là
-
A.
5.
-
B.
6.
-
C.
7.
-
D.
8.
Đáp án : A
Xem lại định nghĩa chất oxi hóa – khử
Có 5 chất và ion vừa có tính oxi hóa và tính khử là: S, FeO, SO2, Fe2+, HCl
Loại phản ứng nào sau đây luôn không phải là phản úng oxi hóa – khử ?
-
A.
Phản ứng phân hủy
-
B.
Phản ứng trao đổi
-
C.
Phản ứng thế trong hóa học vô cơ
-
D.
Phản ứng hóa học
Đáp án : B
Phản ứng trao đổi không phải là phản ứng oxi hóa - khử.
Hòa tan 12,6 gam Fe bằng dung dịch H2SO4 loãng dư, thu được dung dịch X. Dung dịch X phản ứng vừa đủ với V ml dung dịch KMnO4 0,5M. Giá trị của V là
-
A.
180.
-
B.
90
-
C.
45
-
D.
135
Đáp án : B
HS có thể giải theo cách viết PTHH hoặc theo phương pháp bảo toàn e.
Cách 1:
\(\begin{gathered}
Fe + {H_2}S{O_4} \to FeS{O_4} + {H_2} \hfill \\
0,225\,\,\,\,\,\,\,\,\,\, \to \,\,\,\,\,\,\,0,225\,\,\,\,\,\,\,\,\,\,\,\,\,(mol) \hfill \\
10FeS{O_4} + 2KMn{O_4} + 8{H_2}S{O_4} \to 5F{e_2}{(S{O_4})_3} + 2MnS{O_4} + {K_2}S{O_4} + 8{H_2}O \hfill \\
0,225\,\,\,\,\,\,\,\,\, \to 0,045(mol) \hfill \\
\end{gathered} \)
Cách 2:
\(Fe\xrightarrow{{{H_2}S{O_4}\,loang}}\mathop {Fe}\limits^{ + 2} \xrightarrow{{KMn{O_4}}}\mathop {Fe}\limits^{ + 3} \)
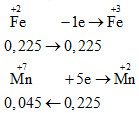
=> V dd KMnO4 = 0,045 : 0,5 = 0,09 lít = 90 ml
Trong phản ứng đốt cháy CuFeS2 tạo ra các sản phẩm CuO, Fe2O3 và SO2 thì 1 phân tử CuFeS2 sẽ
-
A.
nhường 13e.
-
B.
nhận 12e.
-
C.
nhận 13e.
-
D.
nhường 12e.
Đáp án : A
Xét quá trình cho e:
$CuF\text{e}{{\text{S}}_{2}}\,\,\to \,\,\overset{+2}{\mathop{Cu}}\,O+{{\overset{+3}{\mathop{F\text{e}}}\,}_{2}}{{O}_{3}}+\overset{+4}{\mathop{S}}\,{{O}_{2}}+12\text{e}$
Ta có bán phản ứng: CuFeS2 → Cu2+ + Fe3+ + 2S4+ + 13e
Vậy 1 phân tử CuFeS2 nhường 13e
Cho 29,6 gam hỗn hợp X gồm Fe, Mg, Cu theo tỉ lệ mol 1 : 2 : 3 bằng H2SO4 đặc nguội được dung dịch Y và 11,2 lít SO2 (đktc). Cô cạn dung dịch Y được khối lượng muối khan là
-
A.
72 gam
-
B.
21,2 gam
-
C.
43,4 gam
-
D.
36,5 gam
Đáp án : A
Gọi x là số mol Fe trong hỗn hợp X => nMg = 2x, nCu = 3x
=> 56x + 24.2x + 64.3x = 29,6 => x = 0,1 mol
+) Do axit H2SO4 đặc nguội, nên sắt không phản ứng.
+) SO42- + 2e → S+4 => tính số mol e trao đổi => số mol gốc SO42-
+) mmuối = mCu + mMg + ${{m}_{SO_{4}^{2-}}}$
Gọi x là số mol Fe trong hỗn hợp X => nMg = 2x, nCu = 3x
=> 56x + 24.2x + 64.3x = 29,6 => x = 0,1 mol
=> nFe = 0,1 mol, nMg = 0,2 mol, nCu = 0,3 mol
Do axit H2SO4 đặc nguội, nên sắt không phản ứng.
SO42- + 2e → S+4
1 → $\frac{11.2}{22,4}$
=> mmuối = mCu + mMg + ${{m}_{SO_{4}^{2-}}}$ = mCu + mMg + 96.$\frac{1}{2}\sum{{}}$etrao đổi
= 64.0,3 + 24.0,2 + 96.$\frac{1}{2}$1 = 72 gam
Một hỗn hợp gồm hai bột kim loại Mg và Al được chia thành hai phần bằng nhau:
- Phần 1: cho tác dụng với HCl dư thu được 3,36 lít H2.
- Phần 2: hoà tan hết trong HNO3 loãng dư thu được V lít một khí không màu, hoá nâu trong không khí .
Biết các thể tích khí đều đo ở đktc, giá trị của V là
-
A.
2,24 lít.
-
B.
3,36 lít.
-
C.
4,48 lít.
-
D.
5,6 lít.
Đáp án : A
+) Bảo toàn e: ne cho = ne nhận = $2.{{n}_{{{H}_{2}}}}$
+) ne cho (phần 2) = ne cho (phần 1)
+) Bảo toàn e: ne cho (phần 2) = 3.nNO => nNO
Phần 1: ${{n}_{{{H}_{2}}}}=0,15\,\,mol$
Bảo toàn e: ne cho = ne nhận = $2.{{n}_{{{H}_{2}}}}=0,3\,\,mol$
Vì số mol của Mg và Al ở 2 phần bằng nhau và Mg, Al phản ứng với HCl hay với HNO3 đều có số oxi hóa như nhau
=> ne cho (phần 2) = ne cho (phần 1) = 0,3 mol
Phần 2: khí không màu, hóa nâu trong không khí là NO
Bảo toàn e: ne cho (phần 2) = 3.nNO => nNO = 0,3 / 3 = 0,1 mol
=> VNO = 0,1.22,4 = 2,24 lít
Điện phân nóng chảy muối clorua kim loại kiềm, thu được 0,896 lít khí (đktc) và 3,12 gam kim loại. Công thức của muối là:
-
A.
LiCl
-
B.
KCl
-
C.
NaCl
-
D.
RbCl
Đáp án : B
Đặt công thức muối là MCl
tính theo phương trình hóa học rồi tìm nguyên tử khối của kim loại
Đặt CTHH của muối là MCl
Thì ta có: \(2MCl\xrightarrow{dpnc}2M+C{{l}_{2}}\)
Ta có số mol khí Cl2 là 0,04 mol
Suy ra số mol kim loại là 0,08 mol
Vì thế M = \(\frac{3,12}{0,08}\) = 39 (K)
Cho 15,2 gam hỗn hợp X gồm Mg và Ca phản ứng vừa đủ với 8,96 lít (đktc) hỗn hợp khí Y gồm Cl2 và O2 thu được 39,7 gam chất rắn Z chỉ gồm các muối clorua và các oxit kim loại. Khối lượng của Mg trong 15,2 gam X là
-
A.
4,8 gam.
-
B.
7,2 gam.
-
C.
9,2 gam.
-
D.
3,6 gam.
Đáp án : B
Bảo toàn khối lượng, bảo toàn e.
Đặt nCl2 = x; nO2 = y (mol)
BTKL: mY= mZ – mX = 39,7 – 15,2 = 24,5 (g)
Ta có hệ:
\(\left\{ \begin{gathered}
x + y = 0,4 \hfill \\
71x + 32y = 24,5 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x = 0,3 \hfill \\
y = 0,1 \hfill \\
\end{gathered} \right.\)
Đặt nMg = a; nCa = b (mol)
Ta có hệ:
\(\left\{ \begin{gathered}
{m_{Mg}} + {m_{Ca}} = {m_X} \hfill \\
\xrightarrow{{BT:e}}2{n_{Mg}} + 2{n_{Ca}} = 2{n_{C{l_2}}} + 4{n_{{O_2}}} \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
24a + 40b = 15,2 \hfill \\
2a + 2b = 2.0,3 + 4.0,1 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
a = 0,3 \hfill \\
b = 0,2 \hfill \\
\end{gathered} \right.\)
=> mMg = 0,3.24 = 7,2 (g)
Hòa tan hoàn toàn m gam Al vào dung dịch HNO3 loãng, dư thu được 1,344 lít khí N2 (đktc) và dung dịch X. Thêm NaOH dư vào dung dịch X và đun sôi thì thu được 1,344 lít khí NH3 (đktc). Giá trị của m là:
-
A.
0,54
-
B.
1,62
-
C.
10,08
-
D.
9,72
Đáp án : D
bảo toàn electron
Vì khi cho NaOH vào dd X thì tạo ra khí NH3 nên phản ứng tạo muối NH4NO3
Ta có sơ đồ:
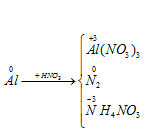
Quá trình cho e: Al → Al+3 + 3e
Quá trình nhận e: 2N+5 +10e → N2
N+5 + 8e → N-3
Số mol khí N2 là 0,06 mol
Số mol khí NH3 là 0,06 mol
Ta có NH4NO3 + NaOH → NaNO3 + NH3 +H2O
Số mol NH4NO3 là 0,06 mol
Áp dụng định luật bảo toàn e thì 3nAl = 10.0,06 + 8.0,06 => nAl = 0,36 mol
Khối lượng của Al là 0,36.27 = 9,72 gam
